Παγκόσμια πρώτη: Εσωσαν ένα μωρό ξαναγράφοντας το DNA του
Παγκόσμια πρώτη: Εσωσαν ένα μωρό ξαναγράφοντας το DNA του
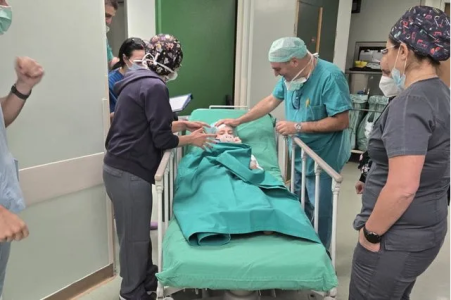
Οταν ο Κέι Τζέι Μαλντούν ήρθε στον κόσμο, οι γιατροί δεν άργησαν να καταλάβουν ότι κάτι δεν πήγαινε καλά. Ισως ήταν μηνιγγίτιδα, ίσως σηψαιμία. Αυτές ήταν οι πρώτες εικασίες των επιστημόνων, όπως σημειώνουν οι New York Times.
Η απάντηση ήρθε όταν ο μικρός Κέι Τζέι (KJ) ήταν μόλις μιας εβδομάδας. Επασχε από μια σπάνια γενετική διαταραχή, την ανεπάρκεια CPS1, η οποία προσβάλλει μόλις ένα στα 1,3 εκατομμύρια νεογνά. Αν κατάφερνε να επιβιώσει, θα αντιμετώπιζε σοβαρά νοητικά και αναπτυξιακά προβλήματα και αργά ή γρήγορα θα χρειαζόταν μεταμόσχευση ήπατος. Ομως τα μισά βρέφη με τη συγκεκριμένη πάθηση πεθαίνουν μέσα στην πρώτη εβδομάδα ζωής.
Οι γιατροί στο Παιδιατρικό Νοσοκομείο της Φιλαδέλφειας (CHOP) πρότειναν στους γονείς να επιλέξουν «ανακουφιστική φροντίδα», αποφεύγοντας τις επιθετικές θεραπείες μπροστά σε μια δυσοίωνη πρόγνωση. «Τον αγαπούσαμε και δεν θέλαμε να υποφέρει», τονίζει στους New York Times η μητέρα του μικρού, Νικόλ Μαλντούν. Ωστόσο, εκείνη και ο σύζυγός της αποφάσισαν να δώσουν στον γιο τους μια ευκαιρία.
Αντί να εγκαταλείψει τη μάχη, ο μικρός κατάφερε να γράψει ιατρική ιστορία. Σήμερα, σε ηλικία 9½ μηνών, είναι ο πρώτος ασθενής, παγκοσμίως, που υποβλήθηκε σε εξατομικευμένη θεραπεία γονιδιακής επεξεργασίας, σύμφωνα με τους θεράποντες ιατρούς του. Ελαβε θεραπεία φτιαγμένη αποκλειστικά για αυτόν, σχεδιασμένη να ξαναγράψει το DNA του, διορθώνοντας τη δική του μοναδική μετάλλαξη. Οι επιστήμονες που ηγήθηκαν της προσπάθειας παρουσίασαν τη δουλειά τους στο ετήσιο συνέδριο της Αμερικανικής Εταιρείας Κυτταρικής & Γονιδιακής Θεραπείας, ενώ η μελέτη δημοσιεύθηκε ταυτόχρονα στο New England Journal of Medicine.

Οι προεκτάσεις αυτής της θεραπείας ξεπερνούν κατά πολύ την περίπτωση του μικρού, τόνισε ο δρ Πίτερ Μαρκς, μέχρι πρόσφατα υπεύθυνος για τη ρύθμιση της γονιδιακής θεραπείας στον αμερικανικό Οργανισμό Τροφίμων και Φαρμάκων (FDA), παραιτηθείς λόγω διαφωνιών με τον υπουργό Υγείας Ρόμπερτ Κένεντι Τζούνιορ.
Πάνω από 30 εκατ. άνθρωποι στις ΗΠΑ πάσχουν από κάποια από τις 7.000+ σπάνιες γενετικές ασθένειες. Οι περισσότερες είναι τόσο σπάνιες, που καμία φαρμακοβιομηχανία δεν επενδύει στην ανάπτυξη θεραπειών, εξηγούν οι New York Times.
Ομως η περίπτωση του μικρού – βασισμένη σε δεκαετίες κρατικά χρηματοδοτούμενης έρευνας – ανοίγει νέο δρόμο: την ανάπτυξη εξατομικευμένων θεραπειών, χωρίς την ανάγκη πολυετών και δαπανηρών κλινικών δοκιμών.
Η πάθηση του Κέι Τζέι προέκυψε από μία και μόνο μετάλλαξη – ένα λάθος «γράμμα» ανάμεσα στα 3 δισ. του ανθρώπινου γονιδιώματος. Η διόρθωσή του απαιτούσε ακριβή στόχευση μέσω μιας τεχνικής που ονομάζεται γονιδιακή επιδιόρθωση βάσης (base editing). Η γονιδιακή θεραπεία τοποθετήθηκε μέσα σε λιπιδικά νανοσωματίδια, ώστε να προστατευτεί στο αίμα μέχρι να φτάσει στο ήπαρ, όπου θα γινόταν η γενετική διόρθωση. Μέσα στα λιπίδια υπήρχαν οδηγίες για την παραγωγή ενός ενζύμου που επιδιορθώνει το γονίδιο. Επίσης, περιείχαν ένα «μοριακό GPS» –τροποποιημένο με την περίφημη μέθοδο CRISPR της γονιδιακής επεξεργασίας– που ανιχνεύει το DNA έως ότου βρει το συγκεκριμένο σημείο προς διόρθωση.
Η θεραπεία του μικρού σχεδιάστηκε ώστε να εντοπίζει ακριβώς τη δική του μετάλλαξη, αλλά το ίδιο μοντέλο μπορεί να προσαρμοστεί και για άλλες μεταλλάξεις. Μόνο οι οδηγίες του CRISPR χρειάζεται να αλλάξουν — κάτι που θα μείωνε δραστικά το κόστος, «κατά τουλάχιστον μία τάξη μεγέθους», όπως λέει στους New York Times ο δρ Μαρκς. Ο ίδιος χαρακτηρίζει τη μέθοδο «μία από τις πιο μετασχηματιστικές τεχνολογίες» με προοπτικές για τη θεραπεία συχνότερων γενετικών ασθενειών όπως η δρεπανοκυτταρική αναιμία, η κυστική ίνωση, το Χάντινγκτον και η μυϊκή δυστροφία. «Θα μπορούσε να αλλάξει ριζικά το σύστημα υγείας», σημειώνει.
Η ιστορία της εξατομικευμένης θεραπείας του Κέι Τζέι ξεκίνησε το βράδυ της 8ης Αυγούστου, όταν η γενετίστρια δρ Ρεμπέκα Αρενς-Νίκλας από το CHOP επικοινώνησε με τον δρ Κιράν Μουσουνουρού του Πανεπιστημίου της Πενσιλβάνια. Το γενετικό τεστ σε ένα νεογέννητο είχε αποκαλύψει ανεπάρκεια CPS1. Ο Μουσουνουρού εργαζόταν σε θεραπείες για συχνότερες μεταλλάξεις. Ομως για την περίπτωση γνώριζε ότι δεν είχε πολύ χρόνο — ίσως το παιδί να είχε μόλις έξι μήνες ζωής πριν από την εμφάνιση σοβαρής εγκεφαλικής βλάβης ή θανάτου. «Από εκείνη τη στιγμή ξεκινάει το ρολόι στο μυαλό μου», σημειώνει στους NYT και προσθέτει, «αυτό είναι πραγματικότητα. Δεν είναι θεωρία».
Η ασθένεια εμποδίζει την αποβολή της αμμωνίας, υποπροϊόντος του μεταβολισμού των πρωτεϊνών, η οποία περνά στο αίμα και φτάνει στον εγκέφαλο. Οι γιατροί έβαλαν τον Κέι Τζέι σε αυστηρή δίαιτα και του χορηγούσαν φάρμακο για την απομάκρυνση της αμμωνίας, αλλά παρέμενε σε υψηλό κίνδυνο. Ο Κέι Τζέι ζούσε στο νοσοκομείο υπό συνεχή φροντίδα. Η κατασκευή και δοκιμή της θεραπείας ήταν δύσκολη. «Επρεπε πολλές φορές να αυτοσχεδιάσουμε», παραδέχεται ο Μουσουνουρού.
Συνεργάστηκε με τον Φιόντορ Ούρνοφ του Berkeley, που φρόντισε να μην υπάρχουν ανεπιθύμητες τροποποιήσεις στο DNA. Ο Ούρνοφ συνεργάζεται με την Danaher Corporation, η οποία ανέλαβε να κατασκευάσει τη θεραπεία με ιατρικά πρότυπα. Η Danaher συνεργάστηκε με άλλες θυγατρικές και ερευνητικά ινστιτούτα, καλύπτοντας το κόστος των υλικών. Ο FDA ενέκρινε γρήγορα τη θεραπεία. Δεκάδες ερευνητές αφοσιώθηκαν επί μήνες αποκλειστικά στο έργο αυτό.
«Στο Berkeley κάψαμε “μια δεξαμενή μεσονύκτιου λαδιού” στο μέγεθος του κόλπου του Σαν Φρανσίσκο», είπε ο Ούρνοφ. «Ποτέ ξανά δεν έγινε τόσο γρήγορα παραγωγή κλινικού CRISPR για γενετική πάθηση». Ο δρ Ντέιβιντ Λιου του Χάρβαρντ, που εφηύρε τη μέθοδο επεξεργασίας βάσης, είπε ότι η ταχύτητα ήταν «εκπληκτική». «Κανονικά, αυτά τα βήματα παίρνουν μια δεκαετία ή και παραπάνω».
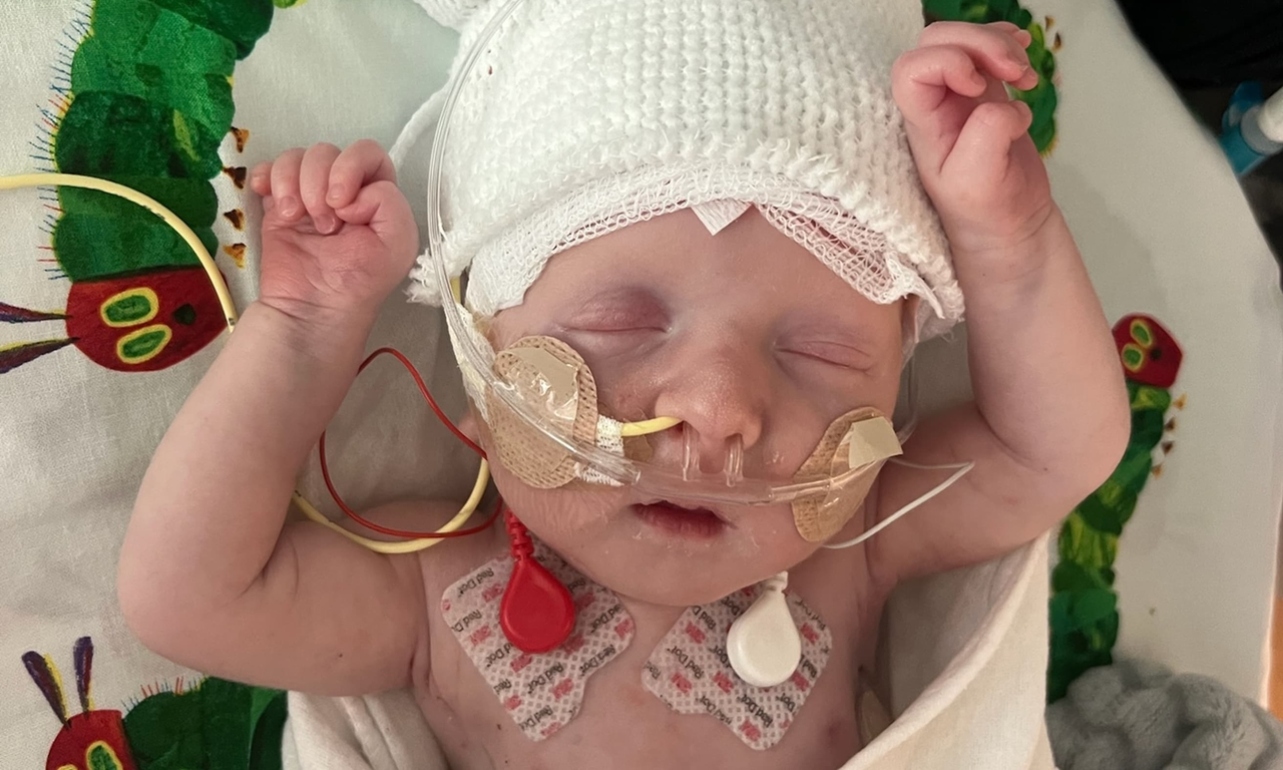
Οταν όλα ήταν έτοιμα, η δρ Αρενς-Νίκλας ενημέρωσε τους γονείς του Κέι Τζέι: «Ενα από τα πιο τρομακτικά μου βήματα ήταν να μπω στο δωμάτιο και να τους πω: “Δεν ξέρω αν θα πετύχει, αλλά υπόσχομαι να κάνω τα πάντα για να είναι ασφαλές”». Στις 25 Φεβρουαρίου, ο μικρός έλαβε την πρώτη έγχυση, πολύ μικρή δόση. Ηταν τότε 6 μηνών. Ο Μουσουνουρού παρακολούθησε την έγχυση, «γεμάτος ενθουσιασμό και φόβο». Ο μικρός κοιμόταν καθ’ όλη τη διάρκεια της διαδικασίας.
Σε δύο εβδομάδες, μπορούσε να καταναλώνει πρωτεΐνη σαν υγιές μωρό. Αλλά εξακολουθούσε να χρειάζεται το φάρμακο. Ελαβε δεύτερη δόση 22 ημέρες μετά. Η δοσολογία του φαρμάκου μειώθηκε στο μισό. Κάποιες ιογενείς λοιμώξεις, που υπό άλλες συνθήκες θα ήταν επικίνδυνες, «τις ξεπέρασε χωρίς πρόβλημα». Πριν από μιάμιση εβδομάδα, έλαβε και τρίτη δόση. Είναι ακόμη νωρίς για να διακοπεί πλήρως το φάρμακο, αλλά η κατάστασή του έχει βελτιωθεί θεαματικά. Ηδη οι γιατροί σχεδιάζουν την έξοδό του από το νοσοκομείο. Αναπτύσσεται κανονικά και το βάρος του έχει φτάσει στο 40ο εκατοστημόριο. Δεν είναι ακόμη βέβαιο αν θα γλιτώσει τη μεταμόσχευση ήπατος.
«Το αποτέλεσμα είναι θρίαμβος για την επένδυση του αμερικανικού λαού στη βιοϊατρική έρευνα», δήλωσε ο Ούρνοφ. Ολοι οι ερευνητές υπογράμμισαν τον καθοριστικό ρόλο της κρατικής χρηματοδότησης: από τη βασική μελέτη βακτηριακών συστημάτων ανοσίας, έως την αποκωδικοποίηση του ανθρώπινου γονιδιώματος, την ανακάλυψη του CRISPR και την κατανόηση της ασθένειας του Κέι Τζέι. «Δεν πιστεύω ότι αυτό θα μπορούσε να είχε συμβεί σε καμία άλλη χώρα πέρα από τις ΗΠΑ», είπε ο Ούρνοφ. «Ολοι μεταξύ μας συμφωνήσαμε: αυτό είναι το πιο σημαντικό πράγμα που έχουμε κάνει ποτέ».
Ακολουθήστε το Protagon στο Google News